Філадельфійська хромосома (Ph-хромосома) — це не просто мікроскопічна аномалія, а фундаментальне відкриття, яке вперше в історії медицини довело генетичну природу раку. Виявлена у 1960 році в мегаполісі Пенсильванії, вона стала “ключем”, що відчинив двері до ери цільової терапії. Ця подія перетворила смертельне білокрів’я на контрольовану недугу, продемонструвавши, як точкова зміна в ланцюгу спадковості може спричинити хаос у всьому організмі. Історія її вивчення — це детектив довжиною в сорок років, де кожен етап наближав людство до розуміння механізмів життя та смерті клітин. Деталі цього епохального відкриття: хто його зробив, як це відбулося, наслідки для всіх хворих на лейкемію та ліки від недуги на iphiladelphia.net.
Випадковий тріумф у Fox Chase
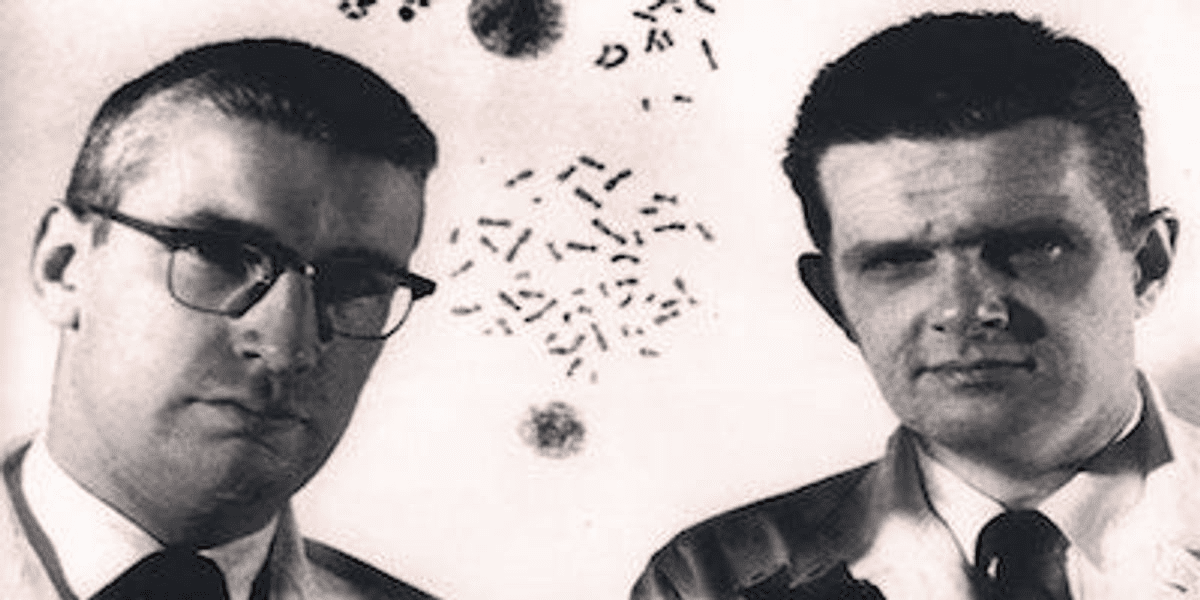
Усе розпочалося у стінах наукового центру Fox Chase, де двоє молодих фахівців — Пітер Новелл з Університету Пенсильванії та Девід Хангерфорд — проводили рутинні спостереження за клітинами пацієнтів, хворих на хронічний мієлоїдний лейкоз (ХМЛ). У ті часи генетика була лише допоміжною дисципліною, а вчені навіть не мали досконалих методів забарвлення препаратів. Проте гострий зір дослідників дозволив помітити дивну деталь: у білих кров’яних тільцях незмінно бракувало частини генетичного матеріалу.
Вони зафіксували, що двадцять друга пара хромосом у хворих виглядала значно коротшою, ніж у здорових людей. Це було перше задокументоване підтвердження того, що специфічна онкопатологія пов’язана з конкретним хромосомним дефектом. Тоді це здавалося неймовірним припущенням, адже панувала думка, що рак викликається виключно вірусами або зовнішніми токсинами. Відкриття Новелла та Хангерфорда спростувало старі догми, заклавши наріжний камінь молекулярної біології в онкологічній практиці.
Анатомія дефекту: народження імені
Оскільки відкриття відбулося в центрі штату Пенсильванія, аномальну структуру офіційно охрестили Філадельфійською хромосомою. Це найменування стало гордістю для міста, закріпивши за ним статус світового лідера в гематологічних розвідках. Протягом наступного десятиліття вчені всього світу намагалися зрозуміти, куди саме зникає фрагмент генетичної одиниці та яку роль це відіграє в розвитку злоякісної патології.
Протягом 1960-х років вивчення генетичного коду нагадувало спробу прочитати книгу через каламутне скло. Технології цитогенетики того часу дозволяли бачити лише розмиті контури хромосом, тому вчені могли зафіксувати лише сам факт “урізання” 22-ї хромосоми. Багато тогочасних скептиків вважали це простою делецією — випадковою втратою фрагмента генетичного коду внаслідок хвороби.
Проте філадельфійські вчені виявили дивовижну наполегливість. Вони довели, що цей дефект не є побічним ефектом руйнування організму, а є стабільним маркером, який зустрічався майже у кожного пацієнта з хронічним мієлолейкозом. Це було перше в історії медицини підтвердження того, що конкретний вид раку викликається мутаціями у певних генах.
Усвідомлення стабільності Ph-хромосоми відкрило двері для нової ери в медицині.
- Точність діагностики. Вперше лікарі отримали можливість підтверджувати рак не лише за симптомами, а й на молекулярному рівні.
- Персоналізований підхід. Філадельфійська хромосома стала, так би мовити, першим “генетичним паспортом” пухлини. Це дозволило коригувати лікування відповідно до індивідуального профілю пацієнта, що згодом призвело до створення таргетної терапії.
- Передвісник революції. Саме на основі вивчення Ph-хромосоми через десятиліття буде створено легендарний препарат Глівек (Іматиніб), який перетворить смертельний рак крові на хронічне захворювання, з яким можна жити повноцінно.
Завдяки наполегливості наукової спільноти Філадельфії, те, що спочатку здавалося лише “дефектом у мікроскопі”, стало фундаментом сучасної онкогенетики. Місто не просто дало ім’я хромосомі — воно дало світу надію на виліковність раку.
Джанет Роулі та велика перестановка
Справжня революція у розумінні природи цього явища відбулася 1973 року завдяки роботі генетикині Джанет Роулі з Чикаго. Використовуючи новітні методи флуоресцентного мічення, вона зробила приголомшливий висновок: генетичний матеріал не зникає безвісти. Насправді відбувається транслокація — взаємний обмін ділянками між дев’ятою та двадцять другою хромосомами.
- Механізм обміну. фрагмент дев’ятої одиниці переміщується на двадцять другу, приєднуючись до гена BCR.
- Результат. створення гібридного “гена-франкенштейна” BCR-ABL, який у звичайному стані не існує в природі.
Цей генетичний “танець” призводить до того, що клітина починає безупинно продукувати специфічний фермент — тирозинкіназу. Цей білок діє як несправний вимикач, який назавжди застряг у положенні “увімкнено”, змушуючи білі кров’яні тільця ділитися з неконтрольованою швидкістю. Саме відкриття Роулі пояснило біологічний двигун лейкемії, давши вченим чітку мішень для майбутніх ліків.

Блокування сигналу: революція Глівеку
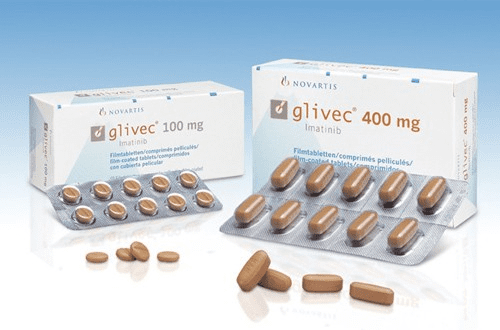
Знаючи ворога в обличчя, науковці розпочали пошук способу вимкнути аномальний протеїн. Наприкінці 1990-х років зусилля Браяна Друкера та інших дослідників привели до появи препарату іматиніб (відомого під назвою Глівек). Це був перший у світі “розумний” засіб, який не вбивав усі клітини поспіль (як традиційна хімієтерапія), а точково блокував лише той самий дефектний фермент, що створюється Філадельфійською хромосомою.
Результати були фантастичними. Пацієнти, чия тривалість життя раніше вимірювалася місяцями, отримали можливість жити десятиліттями, просто приймаючи одну таблетку на день. Це відкриття перетворило фатальне гематологічне захворювання на хронічний стан, подібний до діабету. Глівек довів, що глибоке розуміння генетичної помилки, виявленої колись у Філадельфії, може призвести до створення ідеальної зброї проти онкології.
Нова парадигма онкологічної допомоги
Сьогодні історія Ph-хромосоми вивчається у всіх медичних вишах як зразок наукового методу. Вона довела, що онкологія — це не монолітний монстр, а набір конкретних молекулярних помилок, кожну з яких потенційно можна виправити. Спадщина філадельфійських науковців сформувала концепцію прецизійної медицини, де терапія підбирається індивідуально під мутацію конкретної людини.
Успіх у боротьбі з ХМЛ надихнув на створення сотень інших цільових препаратів для лікування раку легень, молочної залози та меланоми. Тепер дослідники шукають “свою” Філадельфійську хромосому для кожного виду злоякісних новоутворень. Місто, де колись двоє вчених просто уважно подивилися у мікроскоп, назавжди залишиться епіцентром великої інтелектуальної перемоги, що дарує надію мільйонам людей на планеті.

Ключові етапи вивчення Ph-хромосоми
| Рік / Подія | Дійові особи | Науковий та клінічний результат |
| 1960: Виявлення | П. Новелл, Д. Хангерфорд | Відкриття першої генетичної аномалії, пов’язаної з онкологією. |
| 1973: Транслокація | Джанет Роулі | Доказ того, що дефект є обміном генами між 9 та 22 хромосомами. |
| 1980-ті: Гібрид | Група дослідників | Ідентифікація злитого гена BCR-ABL, що запускає недугу. |
| 1990-ті: Глівек | Браян Друкер та ін. | Створення першого інгібітору тирозинкінази (таргетна терапія). |
| Сучасність | Світова спільнота | Перехід до персоналізованої онкології на основі ДНК-профілю. |
Джерела:
- https://www.cancer.gov/publications/dictionaries/cancer-terms/def/philadelphia-chromosome;
- https://geneticeducation.co.in/philadelphia-chromosome-bcr-abl1-fusion-gene-and-its-role-in-cancer/;
- https://www.emedicinehealth.com/is_philadelphia_chromosome_curable/article_em.htm;
- https://easybiologyclass.com/philadelphia-chromosome-and-oncogenic-bcr-abl-gene-translocation-in-cml/.